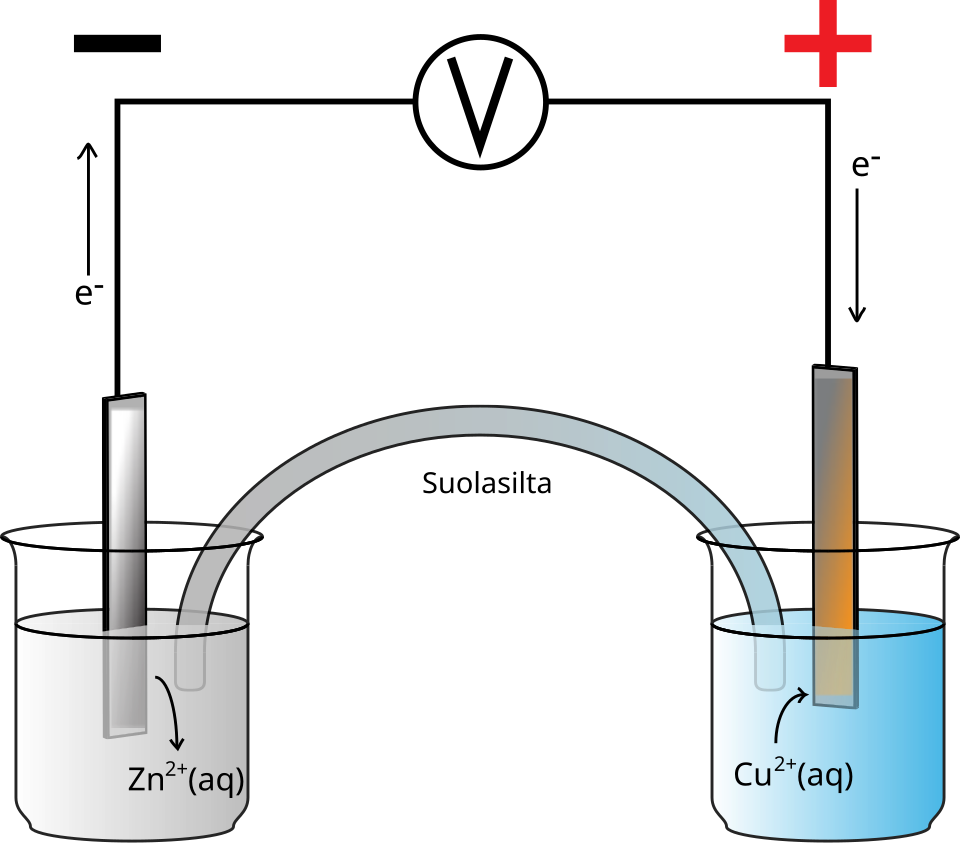
出典:Wikimedia Commons「Daniell cell」
https://commons.wikimedia.org/wiki/File:Daniell_cell.svg
はじめに
電池・電気分解・酸化還元の問題は、公式や計算以前に、反応の起点が曖昧なまま進んで崩れることが多いです。
「どこで何が起こるのか」「電子はどちらへ動くのか」「酸化数は増えるのか減るのか」を、まず最初に確定しましょう。これが確定できないと、式が立たず、計算も迷子になります。
この授業では、酸化還元を“酸素・水素”ではなく“電子”で整理し直し、酸化数の見方・半反応式の扱い・電池と電気分解の共通骨格・計算の核(係数比=モル比)を、できるだけコンパクトな形で揃えていきましょう。
狙いは、知識を増やすことではありません。「引き出すべきルールが起動する順序」を固定して、迷いを減らしましょう。
第1章 「引き出す」段階で勝負が終わる――酸化還元は電子で説明する
酸化還元は、酸素で説明することも、水素で説明することもあります。
ただし、酸化還元の分野として問題を解くときは、中心を電子に置きましょう。電子で整理できれば、酸化数の変化・酸化剤還元剤の関係・電池の極で起きる反応が一本の筋でつながります。
有機化学では、たとえばアルコールからアルデヒド、ケトンへ、という変化を「酸素」「水素」で説明する場面も出てきます。だからこそ、同じ“酸化”という言葉でも、説明の軸がどれなのか(酸素・水素・電子)を見分けられるようにしておきましょう。
一方、酸化還元の問題を解く局面では、電子の話だけでほとんど説明がつくので、電子で考えましょう。
第2章 酸化数は「電荷の感覚」で読む――電子を失うと酸化数が増える
電子はマイナスの電荷を持っています。
そのため、電子を失うということは「マイナスが減る」ことになり、酸化数は増える方向へ動くと捉えましょう。
酸化数は、0、+1、−1のように表しますが、ここで必要なのは「数字の暗記」ではなく、「電荷の感覚」です。
本来の原子の状態よりもマイナスが増えれば、たとえば−1のようにマイナス側へ寄ります。
逆にマイナスが減れば、+1、+2のようにプラス側へ寄ります。
この表し方を見たときに、「プラスに寄っている」「マイナスに寄っている」「電子が余分にある/少なくなった」という感覚を持てるようにしておきましょう。これが、反応の読み取りに直結します。
そして、電子を受け取るとマイナスが増えた状態になるので、酸化数は減る方向へ動きます。
ここまでを、まず“引き出しの手前”に置きましょう。
第3章 酸化剤・還元剤の勘違いを止める――「相手を変える」が先
酸化剤は、相手を酸化させる物質です。
だから酸化剤自身が酸化されるのではありません。酸化剤は相手を酸化させた結果、自分は還元される、と整理しましょう。
同様に、還元剤は相手を還元させ、自分は酸化される、と揃えましょう。
ここでの勘違いが残ったまま電池に入ると、負極・正極の反応を逆に書いたり、電子の流れを逆向きに描いたりして、式の段階で崩れます。
「相手をどう変える役か」を先に置き、そこから自分の変化を確定させましょう。
第4章 酸化数の迅速判定――“速さ”が必要なところだけを先に確定する
酸化数を求める作業は、正確さと同時に速さも必要です。
共通テスト水準では基本ルールで大半を処理できる前提で、迅速判定のルールを揃えておきましょう。
- 単原子イオンは、右上の電荷がそのまま酸化数
- Oは原則−2、Hは原則+1
- 中性化合物は、酸化数の合計が0
例外は存在しますが、まずはこの基本ルールで処理できるところを、迷わず処理しましょう。
第5章 解法手順(圧縮版)――注目元素→増減→必要なら反応式→電子収支へ
酸化還元の問題を解くときは、長い説明よりも「起動順序」を固定することを優先しましょう。
圧縮版として、次の順序で整理しておきます。
5-1 関与物質を抽出して化学式を整える
問題文や図から、酸化還元に直接関与する物質・イオンを抽出し、化学式を整えましょう。
ここが曖昧だと、注目元素も決められません。
5-2 注目元素を決め、酸化数を書いて増減を記録する
Mn、S、Nなど、変化しやすい元素を注目元素として選びましょう。
酸化数を書き、増えたのか減ったのかを記録します。
ここで「酸化」「還元」を確定させましょう。
5-3 必要に応じて反応式を作成し、電子授受数を一致させる
たとえばMn系の例では、KMnO₄中のMnが+7、MnO₂のMnが+4という読みから、+7→+4は電子3個受領を意味します。
電子授受は数が一致するように係数調整し、必要な係数を確定させましょう。
第6章 滴定計算の核――「酸化剤のcV×e-係数比=還元剤のcV×e-係数比」
酸化還元滴定の計算では、係数比(電子の係数比)を確実に適用しましょう。
核となる処理は、次の形で統一しておきます。
- 酸化剤のモル濃度 × 体積 × e⁻係数比 = 還元剤のモル濃度 × 体積 × e⁻係数比
ここで起こりやすいのは、数値の取り違え(濃度や体積)と、係数比の適用ミスです。
mL→Lの換算や、電子係数比(例:1:5など)の適用は、計算の技巧ではなく、ルールの確実運用として扱いましょう。
第7章 電池の整理――「模式図に書き込む」ことで反応と電子の流れを固定する
電池では、負極・正極、溶液中の主要イオン、電子の流れを、模式図に書き込んで整理しましょう。
問題を解くときは、この書き方を実際に使う前提で進めましょう。個別入試でもこの形式が多いので、慣れておきましょう。
7-1 まず確定するもの
- 負極/正極(どちらで酸化・還元が起こるか)
- 溶液(電解液)の種類
- 溶液中の主要イオン
7-2 本質(ここは毎回同じ)
- 負極:電子を放出する酸化反応
- 正極:電子を受け取る還元反応
金属同士の電池では、イオン化傾向が大きい金属ほど負極になりやすい、という整理を用いましょう。
7-3 頻出としての鉛蓄電池
鉛蓄電池は、共通テストというより個別入試で頻出です。ここが解けるようになったら“一人前”という位置づけで、優先度高く扱いましょう。
問題で使われる書き方に慣れておき、反応式と電子の流れを、図に書き込める状態にしていきましょう。
第8章 電気分解の整理――「何が起こりやすいか」を優先順位で固定する
電気分解では、陰極・陽極で何が起こりやすいかの優先順位が曖昧だと、生成物を誤認して式設定が崩れます。
電極材(白金が多い理由=反応しにくい)にも触れつつ、まず“起こりやすい方向”を固定しておきましょう。
8-1 迷ったときの整理
反応対象が乏しい場合、水(H⁺)やOH⁻が関与し、H₂やO₂が発生しやすくなります。
迷ったらH⁺の挙動で整理し、陰極側でH₂発生、陽極側でO₂発生、という見通しで立て直しましょう。
第9章 計算の核――「係数比=モル比」を一貫して使う
計算は、場面ごとに新しい公式を探すのではなく、係数比=モル比で統一しましょう。
求めたい物質のモルを導出し、必要なら体積や質量へ変換します。
滴定と同様に、「受け取った電子mol=放出した電子mol」の一致を、終点・収支の核として押さえましょう。
おわりに(授業内の次アクションに接続)
この回で強調したのは、「引き出すルールが入っていないと絶対に解けない」という点です。
酸化還元は電子、電池は負極=酸化/正極=還元、電気分解は優先順位とH⁺の挙動で立て直す、という骨格をまず固定しましょう。
その上で、計算は係数比=モル比、電子molの一致へ戻しましょう。
復習では、配布プリントとまとめ表を起点に、模式図へ書き込む形で反応の起点を固定していきましょう。

この記事、どう感じましたか? 感想もらえると嬉しいです(^^)