授業日 2025年9月27日
溶解度の計算問題は、大学入試でも頻出分野の一つです。しかし実際には、考え方そのものは中学1年生レベルの一次方程式に帰着します。
つまずきの原因は計算ではなく、溶質・溶媒・溶液の区別と、式の立て方が統一されていないことにあります。
この記事では、溶解度問題を一貫した方法で解くための基本的な考え方と、代表的な問題の処理手順を整理します。
溶解度問題で使う「共通の式」
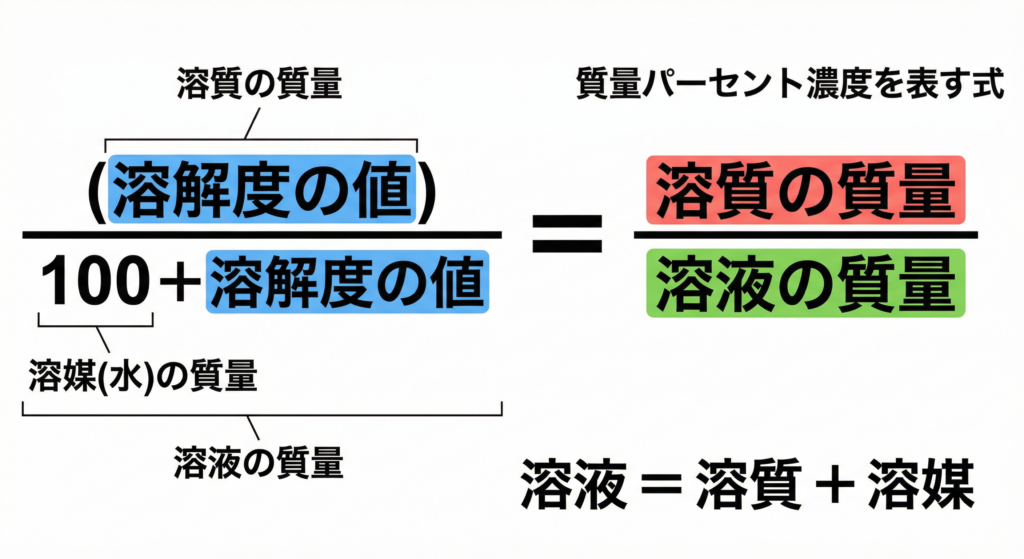
溶解度は通常、
「水(溶媒)100gに対して溶ける溶質の質量」
として与えられます。
この性質をそのまま式にすると、次の比を常に保つことができます。
溶液の質量溶質の質量=100+溶解度溶解度
この形を基準にすれば、
- 冷却による結晶析出
- 蒸発を伴う問題
- 溶液の質量が100gでない場合
もすべて 同じ発想・同じ構造 で処理できます。
質量%濃度の確認(最重要)
溶解度問題では、途中で質量%濃度が問われることがあります。
定義は必ず次の形です。
- 分子:溶質の質量
- 分母:溶液の質量
質量%濃度=溶液溶質×100
ここで
「分母を溶媒にしてしまう」
「溶液と溶質を混同する」
ことが、典型的な失点原因です。
冷却による結晶析出の基本処理
例として、次のような状況を考えます。
- 高温で作った飽和溶液を冷却する
- 温度低下により、溶解度が小さくなる
- 余分な溶質が結晶として析出する
手順の整理
- 初期状態
- 温度と溶解度から、溶質と溶液の比を決める
- 結晶析出量を XXX g とおく
- 最終状態の溶質・溶液の質量を式で表す
- 溶解度の比が成り立つように一次方程式を立てる
結晶が析出すると、
溶質だけでなく溶液全体の質量も減る
ことがポイントです。
蒸発を伴う溶解度問題(硝酸カリウムの例)
蒸発が加わると条件は複雑に見えますが、処理は同じです。
- 溶媒(水)が減る
- その後、結晶が析出する
このとき、
- 溶質の質量
- 溶液全体の質量
を 段階ごとに整理して式に反映 します。
最終的には、
「ある温度での溶解度比(溶質:溶液)」
を満たす一次方程式を解くだけです。
硫酸銅五水和物の溶解度問題
高校化学で特につまずきやすいのが、五水和物を含む溶解度問題です。

参考:Wikimedia Commons
分子量の整理
- CuSO₄ の式量:160
- CuSO₄·5H₂O の分子量:250
結晶が X g 析出した場合、
- 溶質として減るのは CuSO₄ の部分だけ
- 溶質減少量:
一方、結晶が出た分だけ、
- 溶液全体の質量も XXX g 減少
この2点を同時に式に反映させる必要があります。
注意点
- 「結晶=溶質だけが減る」と考えない
- 水和物では 分子量比の意味を必ず意識する
計算自体は煩雑ですが、考え方はこれまでと同一です。
コロイドの基本概念整理
溶解度の計算後は、コロイドに関する基礎用語の確認が重要です。
コロイド粒子の大きさ
- およそ
このスケール感は暗記しておく価値があります。
基本用語
- ゾル:粒子が分散した流動性のある状態
- ゲル:粒子が網目構造を作った半固体
- チンダル現象:光の散乱
- ブラウン運動:粒子の不規則運動
- 透析:半透膜による粒子の分離

参考:Wikimedia Commons
観察装置
- コロイド粒子は通常の光学顕微鏡では観察できない
- 観察には 限外顕微鏡 を用いる
まとめ:溶解度問題を安定して解くために
- 溶質・溶媒・溶液を厳密に区別する
- 溶解度は 「溶質:溶液」の比 で統一する
- 蒸発・析出・水和物も同じ枠組みで処理する
この考え方を徹底すれば、溶解度問題は 特別な入試問題ではなく、処理可能な定型問題になります。
参考資料
本記事は、授業記録および文字起こし資料
「溶解度の計算問題と、コロイドに関する基本概念」
(2025年9月27日実施)をもとに再構成したものです。

この記事、どう感じましたか? 感想もらえると嬉しいです(^^)